Trung tâm Nghiên cứu sản xuất vaccine và sinh phẩm y tế đã tiến hành thử nghiệm giai đoạn 2 trên 240 trẻ tại 10 xã của huyện Thanh Sơn Phú Thọ.
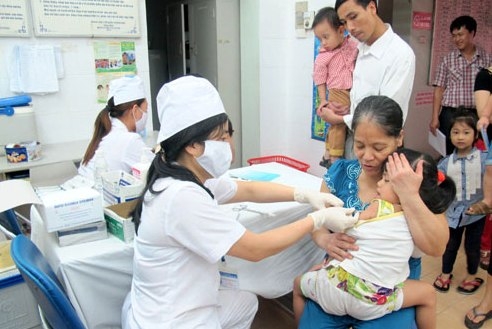 |
| Ảnh minh họa |
Sau khi thử nghiệm giai đoạn 1 trên 60 người lớn khỏe mạnh để đánh giá về tính an toàn của vaccine phòng bệnh bại liệt IPOVAC, Trung tâm Nghiên cứu sản xuất vaccine và sinh phẩm y tế đã tiến hành thử nghiệm giai đoạn 2 trên 240 trẻ tại 10 xã của huyện Thanh Sơn, tỉnh Phú Thọ.
Do đó, trẻ sẽ được tiêm 3 mũi vaccine bại liệt bất hoạt IPOVAC (vaccine bất hoạt là vaccine có kháng nguyên hay phân tử kích thích cơ thể sinh miễn dịch phòng bệnh bại liệt từ những virus bại liệt đã chết), mỗi mũi cách nhau một tháng.
Mỗi trẻ sẽ được lấy máu 3 lần trước khi tiêm mũi 1, trước tiêm mũi 3 và sau tiêm mũi 3 một tháng để đánh giá về tính an toàn, tính sinh miễn dịch của trẻ trước và sau tiêm.
Chỉ những trẻ đáp ứng đủ các tiêu chuẩn được quy định như độ tuổi, cân nặng, không có tiền sử mắc các bệnh suy giảm miễn dịch, chưa uống hoặc tiêm vacxince bại liệt và hoàn toàn khoẻ mạnh.
Đặc biệt phải nhận được sự đồng ý và tình nguyện của các bậc phụ huynh có trẻ tham gia tiêm vacxince IPOVAC.
Tất cả trẻ sau khi tiêm được theo dõi sức khoẻ hằng ngày trong vòng 7 ngày đầu, nhằm ghi nhận tất cả những dấu hiệu, phản ứng của trẻ sau tiêm và hằng tuần trong thời gian tiếp theo.
Theo TS. BS Vũ Đình Thiểm, Trưởng Khoa Dịch tễ, Trưởng Phòng Thử nghiệm lâm sàng (Viện Vệ sinh dịch tễ Trung ương), địa bàn Thanh Sơn, Phú Thọ đã từng triển khai thử nghiệm một số vacxince như viêm não Nhật Bản, Rotavirus. Do đó, cán bộ y tế ở đây có kinh nghiệm trong thực hiện các nghiên cứu, thử nghiệm lâm sàng và khả năng vận động người dân tham gia.
Sau khi kết thúc giai đoạn 1 thành công, giai đoạn 2 sẽ được triển khai từ tháng 12/2015 đến tháng 7/2016. Nếu kết quả đạt yêu cầu về tính an toàn và khả năng sinh miễn dịch thì sẽ tiếp tục triển khai giai đoạn 3 trên gần 1.000 trẻ.
Theo đó đến năm 2018, vacxince bại liệt IPOVAC sẽ có mặt trên thị trường, giúp các bà mẹ có thêm lựa chọn khi cho trẻ khi tiêm chủng.




